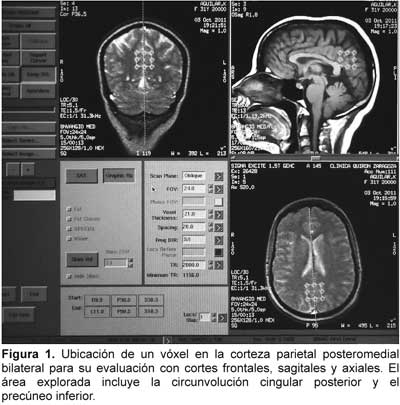
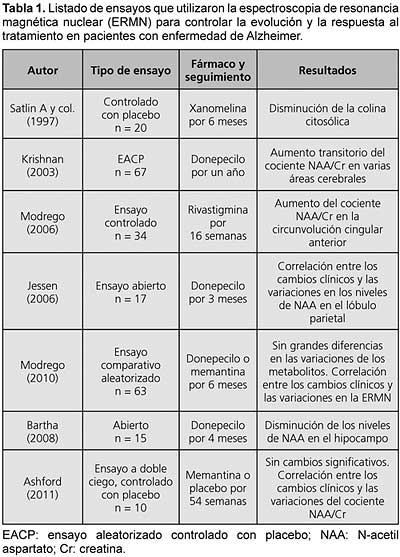
Bibliografía del artículo
Bibliografía del artículo
1. Petersen RC, Smith GE, Waring SC, Ivnik RJ, Tangalos EG, Kokmen E. Mild Cognitive Impairment. Clinical characterization and outcome. Arch Neurol 56:303-308, 1999.
2. Lopez OL, Becker JT, Jagust W, et al. Neuropsychological characteristics of mild cognitive impairment subgroups. J Neurol Neurosurg Psychiatry 77:159-165, 2006.
3. Johnson KA, Jones K, Holman BL. Preclinical prediction of of Alzheimer's disease using SPECT. Neurology 50:1563-1572, 1998.
4. Bennet DA, Wilson RS, Schneider JA, et al. Natural history of mild cognitive impairment in older persons. Neurology 59:198-205, 2002.
5. McKelvey R, Bergman H, Stern J. Lack of prognostic significance of SPECT abnormalities in elderly subjects with a mild memory loss. Can J Neurol Sci 26:23-28, 1999.
6. Krasuki JS, Alexander, Horwitz B, et al. Volumes of medial temporal lobe structures in patients with Alzheimer's disease and mild cognitive impairment (and in healthy controls). Biol Psychiatry 43:60-68, 1998.
7. Morris JC, Storandt M, Miller JP, et al. Mild Cognitive Impairment represents early-stage Alzheimer's disease. Arch Neurol 58:397-405, 2001.
8. Albert MS, DeKosky ST, Dickson D, Dubois B, Feldman HH, Fox NC, Gamst A, Holtzman DM, Jagust WJ, Petersen RC, Snyder PJ, Carrillo MC, Thies B, Phelps CH. The diagnosis of mild cognitive impairment due to Alzheimer's disease: Recommendations of the National Institute on aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease. Alzheimers Dement 7:270-279, 2011.
9. Fayed N, Olmos S, Morales H, Modrego PJ. Physical basis of Magnetic Resonance Spectroscopy and its application to Central Nervous System diseases. Am J Appl Sci 3:1836-1845, 2006.
10. Hsu YY, Chang C, Chang CN, Chu NS, Lim KE, Hsu JC. Proton MR spectroscopy in patients with complex partial seizures: single-voxel spectroscopy versus chemical-shift imaging. AJNR Am J Neuroradiol 20(4):643-51, 1999.
11. Hsu YY, Chen MC, Lim KE, Chang C. Reproducibility of hippocampal single-voxel proton MR spectroscopy and chemical shift imaging. AJR Am J Roentgenol 176(2):529-36, 2000.
12. Maheshwari S, Fatterpeaker G, Castillo M, Mukherji SK. Proton MR spectroscopy of the brain. Semin Ultrasound CT MR 21(6):434-451, 2000.
13. Bonavita S, Di Salle F, Tedeschi G, Proton MRS in neurological disorders. Eur J Radiol 30:125-131, 1999.
14. Burlina A, Aureli T, Bracco F, Conti F, Battistin L. MR spectroscopy: a powerful tool for investigating brain function and neurological diseases. Neurochem Res 2000; 25: 1365-1372.
15. Kantarci K, Petersen RC, Boeve BF, et al. 1H MR spectroscopy in common dementias. Neurology 63:1393-1398, 2004.
16. Kantarci K, Jack CR, Xu YC, et al. Regional metabolic patterns in mild cognitive impairment and Alzheimer's disease. Neurology 55:210-217, 2000.
17. Jessen F, Block W1, Träber F, et al. Proton MR spectroscopy detects a relative decrease on N-acetylaspartate in the medial temporal lobe of patients with AD. Neurology 55:684-688, 2000.
18. Christiansen P, Schlosser A, Henriksen O. Reduced N-acetylaspartate content in the frontal part of the brain in patients with probable Alzheimer's disease. Magn Reson Imaging 13:457-462, 1995.
19. Schuff N, Amend DL, Meyerhoff DJ, Tanabe JL, Norman D, Fein G, Weiner MW. Alzheimer disease: quantitative H-1 MR spectroscopic imaging of frontoparietal brain. Radiology 207:91-102, 1998.
20. Schuff N, Capizzano A, Du AT, Amend DL, O'Neil J, Norman D, Kramer J, Jagust W, Miller B, Wolkowitz OM, Yaffe K, Weiner MW. Selective reduction of N-acetylaspartate in medial temporal and parietal lobes in AD. Neurology 58:928-935, 2002.
21. MacKay S, Meyerhoff DJ, Constans JM, Norman D, Fein G, Weiner MW. Regional gray and white matter metabolic differences in subjects with AD, with subcortical ischemic vascular dementia, and elderly controls with H Magnetic Resonance Spectroscopy Imaging. Arch Neurol 53:167-174, 1996.
22. Miller BL, Moats RA, Shonk T, Earnst E, Wooley S, Ross BD. Alzheimer's disease: depiction of increased cerebral myoinositol with proton MR spectroscopy. Radiology 187:433-437, 1993.
23. Shonk TK, Moats RA, Gifford P, Michaelis T, Mandigo JC, Izumi J, Ross BD. Probable Alzheimer Disease: diagnosis with Proton MR Spectroscopy. Radiology 195:65-72, 1995.
24. Rai GS, McConnel JR, Waldman A, Grant D, Chaudhry M. Brain proton spectroscopy in dementia: an aid to clinical diagnosis. Lancet 353:1063-1064, 1999.
25. Parnetti L, Lowenthal DT, Presciutti O, et al. 1 H-MRS, MRI-based hippocampal volumetry, and 99mTc-HMPAO-SPECT in normal aging, age-associated memory impairment, and probable Alzheimer's disease. J Am Geriatr Soc 44:133-138, 1996.
26. Kantarci K, Xu YC, Shiung MM, et al. Comparative diagnostic utility of different MR modalities in Mild Cognitive Impairment and Alzheimer's disease. Dement Geriatr Cogn Disord 14:198-207, 2002.
27. Modrego PJ, Fayed N, Pina MA. Conversion from mild cognitive impairment to probable Alzheimer's disease predicted by brain Magnetic Resonance Spectroscopy. Am J Psychiatry 162:667-675, 2005.
28. Modrego PJ, Fayed N, Sarasa M. Magnetic Resonance Spectroscopy in the prediction of early conversion from amnestic Mild Cognitive Impairment to dementia. BMJ Open 2011; 1e: 000007. doi: 10.1136/bmjopen-2010-000007.
29. Fayed N, Dávila J, Oliveros A, Castillo J, Medrano JJ. Utility of different MR modalities in mild cognitive impairment and its use as a predictor of conversion to probable dementia. Acad Radiol 15:1089-1098, 2008.
30. Metastasio A, Rinaldi P, Tarducci R, et al. Conversión of MCI to dementia: Role of proton magnetic resonance spectroscopy. Neurobiol Aging 27:926-932, 2005.
31. Targosz-GajniakM, Siuda J, Wicher M, Bujak M, Opala G. Magnetic Resonance Spectroscopy as a predictor of conversion to dementia in mild cognitive impairment. Eur J Neurol 18(2):350 (Abstract), 2011.
32. Kantarci K, Weigand SD, Przybelski SA, et al. Risk of dementia in MCI. Combined effect of cerebrovascular disease, volumetric MRI, and H MRS. Neurology 72:1519-1525, 2009.
33. Pilatus U, Lais C, Rochmont Adu M, et al. Conversion to dementia in mild cognitive impairment is associated with decline of N-acetylaspartate and creatine as revealed by magnetic resonance spectroscopy. Psychiatry Res 173:1-7, 2009.
34. Modrego PJ, Fayed N. Longitudinal MRS in mild cognitive impairment. Am J Alzheimers Dis Other Demen 26:631-636. doi: 10.1177/1533317511433809, 2011.
35. Kantarci K, Knopman DS, Dickson DW, et al. Alzheimer disease: Postmortem neuropathologic correlates of antemortem 1-H MR Spectroscopy metabolite measurements. Radiology 248:210-220, 2008.
36. Godbolt AK, Waldman AD, MacManus DG, Schott JM, Frost C, Cipolotti L, et al. MRS shows abnormalities before symptoms in familial Alzheimer disease. Neurology 66:718-722, 2006.
37. Kantarci K, Boeve BF, Wszolek Z, et al. MRS in presymptomatic MAPT mutation carriers. Neurology 75:771-778, 2010.
38. Kantarci K, Weigand SD, Petersen RC, et al. Longitudinal H MRS changes in mild cognitive impairment and Alzheimer's disease. Neurobiol Aging 28:1330-1339, 2007.
39. Satlin A, Bodick N, Offen WW, Renshaw PF. Brain proton magnetic resonance spectroscopy (1H-MRS) in Alzheimer's disease: changes after treatment with xanomeline, an M1 selective cholinergic agonist. Am J Psychiatry 154:1459-1461, 1997.
40. Frederick B, Satlin A, Wald LL, Hennen J, Bodick N, Renshaw PF. Brain proton magnetic resonance spectroscopy in Alzheimer disease: changes after treatment with xanomeline. Am J Geriatr Psychiatry 10:81-88, 2002.
41. Krishnan RR, Charles HC, Doraiswamy PM (2003), et al. Randomized, placebo-controlled trial of the effects of donepezil on neuronal markers and hippocampal volumes in Alzheimer disease. Am J Psychiatry 160:2003-2011, 2003.
42. Modrego PJ, Pina MA, Fayed N, Díaz M. Changes in metabolite ratios after treatment with rivastigmine in Alzheimer's disease: a nonrandomized controlled trial with magnetic resonance spectroscopy. CNS Drugs 20:867-87, 2006.
43. Jessen F, Traeber F, Freymann K, Maier W, Schild HH, Block W. Treatment monitoring and response prediction with proton MR spectroscopy in AD. Neurology 67:528-530, 2006.
44. Bartha R, Smith M, Rupsingh R, Rylett J, Wells JL, Borrie MJ. High field H MRS of the hippocampus after donepezil treatment in Alzheimer disease. Prog Neuropsychopharmacol Biol Psychiatry 32:786-793, 2008.
45. Modrego PJ, Fayed N, Errea JM, Rios C, Pina MA, Sarasa M. Memantine versus donepezil in mild to moderate Alzheimer's disease: a randomized trial with magnetic resonance spectroscopy. Eur J Neurol 17:405-412, 2010.
46. Ashford JW, Adamson M, Beale T, et al. MR spectroscopy for assessment of memantine treatment in mild to moderate Alzheimer dementia. J Alzheimers Dis 26:331-336, 2011.
47. Schott JM, Frost C, Macmanus DG, Ibrahim F, Waldman AD, Fox ND. Short echo time proton magnetic resonance spectroscopy in Alzheimer's disease: a longitudinal multiple time point study. Brain 133:3315-22, 2010.
48. Antuono PG, Jones JL, Wang Y, Li SJ. Decreased glutamate + glutamine in Alzheimer's disease detected in vivo with (1) H-MRS at 0.5 T. Neurology 56:737-42, 2002.
49. Hattori N, Abe K, Sakoda S, Sawada T. Proton MR spectroscopic study at 3 Tesla on glutamate/glutamine in Alzheimer's disease. Neuroreport 13:183-186, 2002.
50. Rupsingh R, Borrie M, Smith M, Wells JL, Bartha R. Reduced hippocampal glutamate in Alzheimer disease. Neurobiology of Aging 32(5):802-10, 2009.
51. Fayed N, Modrego PJ, Rojas-Salinas G, Aguilar K. Glutamate is decreased in Alzheimer's disease. A magnetic resonance spectroscopy study. Am J Alzheimers Dis Other Demen DOI:10.1177/1533317511421780, 2011.
52. Penner J, Rupsingh R, Smith M, Wells JL, Borrie MJ, Bartha R. Increased glutamate in the hippocampus after galantamine treatment for Alzheimer Disease. Prog Neuropsychopharmacol Biol Psychiatry 34:104-110, 2010.
53. Mega MS. The entorhinal cortex in Alzheimer's disease. J Neurol Neurosurg Psychiatry 71:431-432, 2001.
54. Fayed N, Modrego PJ, Medrano J. Comparative test-retest reliability of metabolite values assessed with Magnetic Resonance Spectroscopy of the brain. The LCModel versus the manufacturer software. Neurol Res 31:472-477, 2009.
55. Nho K, Shen L, Risacher SL, West JD, Foroud T, Jack CR, Weiner MW, Saykin AJ. Automatic prediction of conversion from mild cognitive imapirment to probable Alzheimer's disease using structural magnetic resonance imaging. AMIA Annu Symp Proc 13:542-546, 2010.
56. Devanand DP, Pradhaban G, Liu X, Khandji A, De Santi S, Segal S, Rusinek H, Pelton GH, Honig LS, Mayeux R, Stern Y, Tabert MH, de Leon MJ. Hippocampal and entorhinal atrophy in mild cognitive impairment: prediction of Alzheimer disease. Neurology 68:828-836, 2007.
57. Wang Z, Zhao C, Yu L, Zhou W, Li K. Regional metabolic changes in the hippocampus and posterior cingulated area detected with 3-Tesla Magnetic resonance spectroscopy in patients with mild cognitive impairment and Alzheimer's disease. Acta Radiol 50:312-319, 2009.
58. Caserta MT, Ragin A, Hermida AP, John Ahrens R, Wise L. Single voxel MR spectroscopy at 3T in a memory disorders clinic: early right hippocampal NAA/Cr loss in mildly impaired subjects. Psychiatry Res 164:154-159, 2008.
59. Mandal PK. Magnetic Resonance Spectroscopy (MRS) and its application in Alzheimer's Disease. Concepts in Magnetic Resonance Part A 30:40-65, 2007.
60. Mandal PK. In vivo proton magnetic resonance spectroscopic signal processing for the absolute quantitation of brain metabolites. Eur J Radiol Ahead of print, 2011.
61. Petersen RC, Roberts RO, Knopman DS, Boeve BF, Geda YE, Ivnik RJ, Smith GE, Jack CR. Mild cognitive impairment. Ten years later. Arch Neurol 66:1447-1455, 2010.
62. Modrego PJ, Fayed N, Olmos S. Clinical and radiological differences in Alzheimer's disease with and without a history of mild cognitive impairment. Neuroradiology J 23:659-664, 2010.




 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo> Enviar correspondencia a:
Enviar correspondencia a: